Можно ли пить тяжелую воду
Тяжёлая вода — Википедия
| Тяжёлая вода | |||
|---|---|---|---|
| |||
| Систематическое наименование | оксид дейтерия | ||
| Традиционные названия | тяжёлая вода | ||
| Хим. формула | D2O | ||
| Состояние | жидкость | ||
| Молярная масса | 20,04 г/моль | ||
| Плотность | 1,1042 г/см³ | ||
| Динамическая вязкость | 0,00125 Па·с | ||
| Температура | |||
| • плавления | 3,81 °C | ||
| • кипения | 101,43 °C | ||
| Критическая точка | |||
| • давление | 21,86 МПа | ||
| Мол. теплоёмк. | 84,3 Дж/(моль·К) | ||
| Уд. теплоёмк. | 4,105 Дж/(кг·К) | ||
| Энтальпия | |||
| • образования | −294,6 кДж/моль | ||
| • плавления | 5,301 кДж/моль | ||
| • кипения | 45,4 кДж/моль | ||
| Давление пара | 10 мм рт. ст. при 13,1 °C 100 мм рт. ст. при 54 °C | ||
| Растворимость | |||
| • в воде | неограниченная | ||
| • в эфире | малорастворима | ||
| • в этаноле | неограниченная | ||
| Показатель преломления | 1,32844 (при 20 °C) | ||
| Рег. номер CAS | 7789-20-0 | ||
| PubChem | 24602 | ||
| Рег. номер EINECS | 232-148-9 | ||
| SMILES | |||
| InChI | |||
| RTECS | ZC0230000 | ||
| ChEBI | 41981 | ||
| ChemSpider | 23004 | ||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
| Медиафайлы на Викискладе | |||
Тяжёлая вода́ — обычно этот термин применяется для обозначения тяжеловодородной воды, известной также как оксид дейтерия. Тяжеловодородная вода имеет ту же химическую формулу, что и обычная вода, но вместо двух атомов обычного лёгкого изотопа водорода (протия) содержит два атома тяжёлого изотопа водорода — дейтерия, а её кислород по изотопному составу соответствует кислороду воздуха[1]. Формула тяжеловодородной воды обычно записывается как D2O или 2H2O. Внешне тяжёлая вода выглядит как обычная — бесцветная жидкость без вкуса и запаха. Не радиоактивна.
Молекулы тяжеловодородной воды были впервые обнаружены в природной воде Гарольдом Юри в 1932 году, за что учёный был удостоен Нобелевской премии по химии в 1934 году. Уже в 1933 году Гилберт Льюис впервые выделил чистую тяжеловодородную воду. При электролизе обычной воды, содержащей наряду с обычными молекулами воды незначительное количество молекул полутяжёлой воды (НDО) и ещё меньшее количество молекул тяжёлой воды (D2O), включающих в себя тяжёлый изотоп водорода, остаток постепенно обогащается молекулами этих соединений. Из такого остатка после многократного повторения электролиза Льюису удалось выделить небольшое количество воды, состоящей почти на 100 % из молекул соединения кислорода с дейтерием и получившей название тяжёлой. Этот способ производства тяжёлой воды остаётся основным и сейчас, хотя используется в основном на окончательной стадии обогащения от 5—10 % до >99 % (см. ниже).
После открытия в конце 1938 года деления ядер и осознания возможности использования цепных ядерных реакций деления, индуцированных нейтронами, возникла необходимость в замедлителе нейтронов — веществе, позволяющем эффективно замедлять нейтроны, не теряя их в реакциях захвата. Наиболее эффективно нейтроны замедляются лёгкими ядрами, и самым эффективным замедлителем должны были бы быть ядра обычного водорода (протия), однако они обладают высоким сечением захвата нейтронов. Напротив, тяжёлый водород захватывает очень мало нейтронов (сечение захвата тепловых нейтронов у протия в более чем 100 тысяч раз выше, чем у дейтерия). Технически наиболее удобным соединением дейтерия является тяжёлая вода, причём она способна также служить теплоносителем, отводя выделяющееся тепло от области, где происходит цепная реакция деления. С самых ранних времён ядерной энергетики тяжёлая вода стала важным компонентом в некоторых реакторах, как энергетических, так и предназначенных для наработки изотопов плутония для ядерного оружия. Эти так называемые тяжеловодные реакторы имеют то преимущество, что могут работать на природном (необогащённом) уране без использования графитовых замедлителей, которые на этапе вывода из эксплуатации могут представлять опасность взрыва пыли и содержат наведённую радиоактивность (углерод-14 и ряд других радионуклидов) [2]. Однако в большинстве современных реакторов используется обогащённый уран с нормальной «лёгкой водой» в качестве замедлителя, несмотря на частичную потерю замедленных нейтронов.
Производство тяжёлой воды в СССР[править | править код]
| Эта статья или раздел описывает ситуацию применительно лишь к одному региону (СССР), возможно, нарушая при этом правило о взвешенности изложения. Вы можете помочь Википедии, добавив информацию для других стран и регионов. |
Промышленное производство и применение тяжёлой воды началось с развитием атомной энергетики. В СССР при организации Лаборатории № 3 АН СССР (современный ИТЭФ) перед руководителем проекта А. И. Алихановым была поставлена задача создания реактора на тяжёлой воде. Это обусловило потребность в тяжёлой воде, и техническим советом Специального комитета при СНК СССР был разработан проект Постановления СНК СССР «О строительстве полупромышленных установок по производству продукта 180», работы по созданию производительных установок тяжёлой воды в кратчайшие сроки были поручены руководителю атомного проекта Б. Л. Ванникову, народному комиссару химической промышленности М. Г. Первухину, представителю Госплана Н. А. Борисову, народному комиссару по делам строительства СССР С. З. Гинзбургу, народному комиссару машиностроения и приборостроения СССР П. И. Паршину и народному комиссару нефтяной промышленности СССР Н. К. Байбакову [3]. Главным консультантом в вопросах тяжёлой воды стал начальник сектора Лаборатории № 2 АН СССР М. И. Корнфельд.
| Параметр | D2O | HDO | H2O |
|---|---|---|---|
| Температура плавления, °C | 3,82 | 2,04 | 0,00 |
| Температура кипения, °C | 101,4 | 100,7 | 100,0 |
| Плотность при 20 °C, г/см³ | 1,1056 | 1,054 | 0,9982 |
| Температура максимальной плотности, °C | 11,6 | 4,0 | |
| Вязкость при 20 °C, сантипуаз | 1,2467 | 1,1248 | 1,0016 |
| Поверхностное натяжение при 25 °C, дин·см | 71,87 | 71,93 | 71,98 |
| Молярное уменьшение объёма при плавлении, см³/моль | 1,567 | 1,634 | |
| Молярная теплота плавления, ккал/моль | 1,515 | 1,436 | |
| Молярная теплота парообразования, ккал/моль | 10,864 | 10,757 | 10,515 |
| pH при 25 °C | 7,41 | 7,266 | 7,00 |
В природных водах один атом дейтерия приходится на 6400—7600[5] атомов протия. Почти весь он находится в составе молекул полутяжёлой воды DHO, одна такая молекула приходится на 3200—3800 молекул лёгкой воды. Лишь очень незначительная часть атомов дейтерия формирует молекулы тяжёлой воды D2O, поскольку вероятность двум атомам дейтерия встретиться в составе одной молекулы в природе мала (примерно 0,5⋅10−7). При искусственном повышении концентрации дейтерия в воде эта вероятность растёт.
Биологическая роль и физиологическое воздействие[править | править код]
Тяжёлая вода токсична лишь в слабой степени, химические реакции в её среде проходят несколько медленнее по сравнению с обычной водой, водородные связи с участием дейтерия несколько сильнее обычных. Эксперименты над млекопитающими (мыши, крысы, собаки)[6] показали, что замещение 25 % водорода в тканях дейтерием приводит к стерильности, иногда необратимой[7][8]. Более высокие концентрации приводят к быстрой гибели животного; так, млекопитающие, которые пили тяжёлую воду в течение недели, погибли, когда половина воды в их теле была дейтерирована; рыбы и беспозвоночные погибают лишь при 90 % дейтерировании воды в теле[9]. Простейшие способны адаптироваться к 70 % раствору тяжёлой воды, а водоросли и бактерии способны жить даже в чистой тяжёлой воде[6][10][11][12][13]. Человек может без видимого вреда для здоровья выпить несколько стаканов тяжёлой воды, весь дейтерий будет выведен из организма через несколько дней. Так, в одном из экспериментов по изучению связи вестибулярного аппарата и непроизвольных движений глаз (нистагма) добровольцам предлагалось выпить от 100 до 200 граммов тяжёлой воды; в результате поглощения более плотной тяжёлой воды купулой (желатинообразной структурой в полукружных каналах) её нейтральная плавучесть в эндолимфе каналов нарушается, и возникают лёгкие нарушения пространственной ориентации, в частности нистагм. Этот эффект аналогичен возникающему при приёме алкоголя (однако в последнем случае плотность купулы уменьшается, поскольку плотность этилового спирта меньше плотности воды)[14].
Таким образом, тяжёлая вода гораздо менее токсична, чем, например, поваренная соль. Тяжёлая вода использовалась для лечения артериальной гипертензии у людей в суточных дозах от 10 до 675 г D2O в день[15].
В человеческом организме содержится в качестве естественной примеси столько же дейтерия, сколько в 5 граммах тяжёлой воды; этот дейтерий в основном входит в молекулы полутяжёлой воды HDO, а также во все прочие биологические соединения, в которых есть водород.[источник не указан 614 дней]
Тяжёлая вода накапливается в остатке электролита при многократном электролизе воды. На открытом воздухе тяжёлая вода быстро поглощает пары обычной воды, поэтому можно сказать, что она гигроскопична. Производство тяжёлой воды очень энергоёмко, поэтому её стоимость довольно высока. В 1935 году, сразу после открытия тяжёлой воды, её цена составляла ориентировочно 19 долларов за грамм[16]. В настоящее время тяжёлая вода с содержанием дейтерия 99 % ат., продаваемая поставщиками химических реактивов, при покупке 1 кг сто́ит около 1 евро за грамм[17], однако эта цена относится к продукту с контролируемым и гарантированным качеством химического реактива; при снижении требований к качеству цена может быть на порядок ниже.
Среди населения бытует миф о том, что при длительном кипячении природной воды концентрация тяжёлой воды в ней повышается, что якобы может вредно сказаться на здоровье, из-за публикации предположения В. В. Похлёбкина в книге «Чай. Его типы, свойства, употребление», вышедшей в 1968 году[18]. В действительности повышение концентрации тяжёлой воды при кипячении ничтожно. Академик Игорь Васильевич Петрянов-Соколов как-то подсчитал, сколько воды должно испариться из чайника, чтобы в остатке заметно повысилось содержание дейтерия. Оказалось, что для получения 1 литра воды, в которой концентрация дейтерия равна 0,15 %, то есть всего в 10 раз превышает природную, в чайник надо долить в общей сложности 2,1⋅1030 тонн воды, что в 300 млн раз превышает массу Земли[19]. Гораздо сильнее сказывается на вкусе и свойствах воды при кипячении повышение концентрации растворённых солей, переход в раствор веществ из стенок посуды и термическое разложение органических примесей.
Стоимость производства тяжёлой воды определяется затратами энергии. Поэтому при обогащении тяжёлой воды применяют последовательно разные технологии — вначале пользуются более дешёвыми технологиями, с бо́льшими потерями тяжёлой воды, а в конце — более энергозатратными, но с меньшими потерями тяжёлой воды.
С 1933 по 1946 годы единственным применявшимся методом обогащения был электролиз. В последующем появились технологии ректификации жидкого водорода и изотопного обмена в системах: водород — жидкий аммиак, водород — вода, сероводород — вода. Современное массовое производство во входном потоке использует воду, дистиллированную из электролита цехов получения электролитического водорода, с содержанием 0,1—0,2 % тяжёлой воды.
На первой стадии концентрирования применяется двухтемпературная противоточная сероводородная технология изотопного обмена, выходная концентрация тяжёлой воды 5—10 %. На второй — каскадный электролиз раствора щёлочи при температуре около 0 °C, выходная концентрация тяжёлой воды 99,75—99,995 %.
Крупнейшим в мире производителем тяжёлой воды является Канада, что связано с применением в её энергетике тяжеловодных ядерных реакторов CANDU.
Важнейшим свойством тяжёловодородной воды является то, что она практически не поглощает нейтроны, поэтому используется в ядерных реакторах для замедления нейтронов и в качестве теплоносителя. Она используется также в качестве изотопного индикатора в химии, биологии и гидрологии, агрохимии и др. (в том числе в опытах с живыми организмами и при диагностических исследованиях человека). В физике элементарных частиц тяжёлая вода используется для детектирования нейтрино; так, крупнейший детектор солнечных нейтрино SNO (Канада) содержит 1000 тонн тяжёлой воды.
Дейтерий — ядерное топливо для энергетики будущего, основанной на управляемом термоядерном синтезе. В первых энергетических реакторах такого типа предполагается осуществить реакцию D + T → 4He + n + 17,6 МэВ[20].
В некоторых странах (например, в Австралии) коммерческий оборот тяжёлой воды поставлен под государственные ограничения, что связано с теоретической возможностью её использования для создания «несанкционированных» реакторов на природном уране, пригодных для наработки оружейного плутония.
Полутяжёлая вода[править | править код]
Выделяют также полутяжёлую воду (известную также под названиями дейтериевая вода, монодейтериевая вода, гидроксид дейтерия), у которой только один атом водорода замещён дейтерием. Формулу такой воды записывают так: DHO или ²HHO. Следует отметить, что вода, имеющая формальный состав DHO, вследствие реакций изотопного обмена реально будет состоять из смеси молекул DHO, D2O и H2O (в пропорции примерно 2:1:1). Это замечание справедливо и для THO и TDO.
Сверхтяжёлая вода[править | править код]
Сверхтяжёлая вода содержит тритий, период полураспада которого более 12 лет. По своим свойствам сверхтяжёлая вода (T2O) ещё заметнее отличается от обычной: кипит при 104 °C, замерзает при +9 °C и имеет плотность 1,21 г/см³[21]. Известны (то есть получены в виде более или менее чистых макроскопических образцов) все девять вариантов сверхтяжёлой воды: THO, TDO и T2O с каждым из трёх стабильных изотопов кислорода (16O, 17O и 18O). Иногда сверхтяжёлую воду называют просто тяжёлой водой, если это не может вызвать путаницы. Сверхтяжёлая вода имеет высокую радиотоксичность.
Тяжелокислородные изотопные модификации воды[править | править код]
Термин тяжёлая вода применяют также по отношению к тяжелокислородной воде, у которой обычный лёгкий кислород 16O заменён одним из тяжёлых стабильных изотопов 17O или 18O. Тяжёлые изотопы кислорода существуют в природной смеси, поэтому в природной воде всегда есть примесь обеих тяжелокислородных модификаций. Их физические свойства также несколько отличаются от свойств обычной воды; так, температура замерзания 1H218O составляет +0,28 °C[4].
Тяжелокислородная вода, в частности, 1H218O, используется в диагностике онкологических заболеваний (из неё на циклотроне получают изотоп фтор-18, который используют для синтеза препаратов для диагностики онкозаболеваний, в частности 18-фдг).
Общее число изотопных модификаций воды[править | править код]
Если подсчитать все возможные нерадиоактивные соединения с общей формулой Н2О, то общее количество возможных изотопных модификаций воды всего девять (так как существует два стабильных изотопа водорода и три — кислорода):
- Н216O − лёгкая вода, или просто вода
- Н217O
- Н218O − тяжелокислородная вода
- HD16O − полутяжёлая вода
- HD17O
- HD18O
- D216O − тяжёлая вода
- D217O
- D218O
С учётом трития их число возрастает до 18:
- T216O — сверхтяжёлая вода
- T217O
- T218O
- DT16O
- DT17O
- DT18O
- HT16O
- HT17O
- HT18O
Таким образом, кроме обычной, наиболее распространённой в природе «лёгкой» воды 1H216O, в общей сложности существует 8 нерадиоактивных (стабильных) и 9 радиоактивных «тяжёлых вод».
Всего же общее число возможных «вод» с учётом всех известных изотопов водорода (7) и кислорода (17) формально равняется 476. Однако распад почти всех радиоактивных изотопов водорода и кислорода происходит за секунды или доли секунды (важным исключением является тритий, период полураспада которого более 12 лет). Например, все более тяжёлые, чем тритий, изотопы водорода живут порядка 10−20 с; за это время никакие химические связи просто не успевают образоваться, и, следовательно, молекул воды с такими изотопами не бывает. Радиоизотопы кислорода имеют периоды полураспада от нескольких десятков секунд до наносекунд. Поэтому макроскопические образцы воды с такими изотопами получить невозможно, хотя молекулы и микрообразцы могут быть получены. Интересно, что некоторые из этих короткоживущих радиоизотопных модификаций воды легче, чем обычная «лёгкая» вода (например, 1H215O).
- ↑ Петрянов И. В. Самое необыкновенное вещество // Химия и жизнь. — 1965. — № 3. — С. 2—14.
- ↑ http://www-pub.iaea.org/MTCD/publications/PDF/ngwm-cd/PDF-Files/paper%2017%20%28Holt%29.pdf
- ↑ документа Протокол № 9 заседания Специального комитета при Совнаркоме СССР. Москва, Кремль 30 ноября 1945 года в Викитеке
- ↑ 1 2 Water properties
- ↑ Зельвенский Я. Д. Дейтерий // Химическая энциклопедия: в 5 т. / И. Л. Кнунянц (гл. ред.). — М.: Советская энциклопедия, 1990. — Т. 2: Даффа—Меди. — С. 16—17. — 671 с. — 100 000 экз. — ISBN 5-85270-035-5.
- ↑ 1 2 D. J. Kushner, Alison Baker, and T. G. Dunstall. Pharmacological uses and perspectives of heavy water and deuterated compounds (англ.) // Can. J. Physiol. Pharmacol. (англ.)русск. : journal. — 1999. — Vol. 77, no. 2. — P. 79—88. — doi:10.1139/cjpp-77-2-79. — PMID 10535697.
- ↑ Лобышев В. Н., Калиниченко Л. П. Изотопные эффекты D2O в биологических системах. — М.: Наука, 1978. — 215 с.
- ↑ Vertes A. Physiological effects of heavy water. Elements and isotopes: formation, transformation, distribution (англ.). — Dordrecht: Kluwer Acad. Publ., 2004. — 112 p.
- ↑ Trotsenko, Y. A., Khmelenina, V. N., Beschastny, A. P. (1995) The Ribulose Monophosphate (Quayle) Cycle: News and Views. Microbial Growth on C1 Compounds, in: Proceedings of the 8th International Symposium on Microbial Growth on C1 Compounds (Lindstrom M. E., Tabita F. R., eds.). San Diego (USA), Boston: Kluwer Academic Publishers, pp. 23-26
- ↑ Мосин О. В., Швец В. И., Складнев Д. А., Игнатов И. Микробный синтез дейтерий-меченного L-фенилаланина факультативной метилотрофной бактерией Brevibacterium Methylicum на средах с различными концентрациями тяжелой воды // Биофармацевтический журнал. — 2012. — Т. 4, вып. 1. — С. 11—22.
- ↑ Мосин О. В., Игнатов И. Изотопные эффекты дейтерия в клетках бактерий и микроводорослей при росте на тяжелой воде (D2O) // Вода: химия и экология. — 2012. — Вып. 3. — С. 83—94.
- ↑ Crespi H. L. Fully deuterated microorganisms: tools in magnetic resonance and neutron scattering. Synthesis and Applications of Isotopically Labeled Compounds / in: Proceedings of an International Symposium. Baillie T, Jones J.R eds. Amsterdam: Elsevier. 1989. pp. 329—332.
- ↑ Mosin O. V., Ignatov I. Microbiological Synthesis of 2H-Labeled Phenylalanine, Alanine, Valine, and Leucine/Isoleucine with Different Degrees of Deuterium Enrichment by the Gram-Positive Facultative Methylotrophic Bacterium Вrevibacterium Methylicum (англ.) // International Journal of BioMedicine. — 2013. — Vol. 3, iss. 2. — P. 132—138.
- ↑ Money K. E., Myles W. S. Heavy water nystagmus and effects of alcohol (англ.) // Nature. — 1974. — Vol. 247, no. 5440. — P. 404—405. — doi:10.1038/247404a0. — Bibcode: 1974Natur.247..404M. — PMID 4544739.
- ↑ Патент США № 5 223 269 от 29 июня 1993. Method and composition for the treatment of hypertension. Описание патента на сайте Ведомства по патентам и товарным знакам США.
- ↑ Pharmacologist drinks heavy water in experiment (англ.) (недоступная ссылка). Science News Staff (9 February 1935). Дата обращения 7 сентября 2013. Архивировано 9 сентября 2013 года.
- ↑ Deuterium oxide, 99 atom % D | D2O | Sigma-Aldrich
- ↑ Дейтерий — в чайнике? // Химия и жизнь. — 1969. — № 2. — С. 24—25.
- ↑ Илья Леенсон. Тяжелая вода (неопр.). Энциклопедия Кругосвет. Дата обращения 7 сентября 2013.
- ↑ Андреев Б. М., Зельвенский Я. Д., Катальников С. Г. Тяжелые изотопы водорода в ядерной технике. — М.: Энергоатомиздат, 1987.
- ↑ Зельвенский Я. Д. Тритий // Химическая энциклопедия: в 5 т. / Н. С. Зефиров (гл. ред.). — М.: Большая Российская энциклопедия, 1998. — Т. 5: Триптофан—Ятрохимия. — С. 5—7. — 783 с. — 10 000 экз. — ISBN 5-85270-310-9.
Что такое тяжелая вода и можно ли ее пить (4 фото)

Тем, чьи знания по химии ограничиваются объемом школьной программы, может казаться, что вода состоит только из монооксида водорода и имеет всем известную формулу h3O. Это так, но кроме него в состав могут входить изотопы Н: протий, дейтерий и тритий.
Тритий нестабилен, поэтому практически отсутствует в воде. При этом существующий сверхтяжелый водород распадается на гелий, излучая электрон и антинейтрино. Выделение значительного числа электронов может вызвать свечение люминофора вроде того, как светятся небольшие тритиевые брелки, в которых запечатан изотоп.
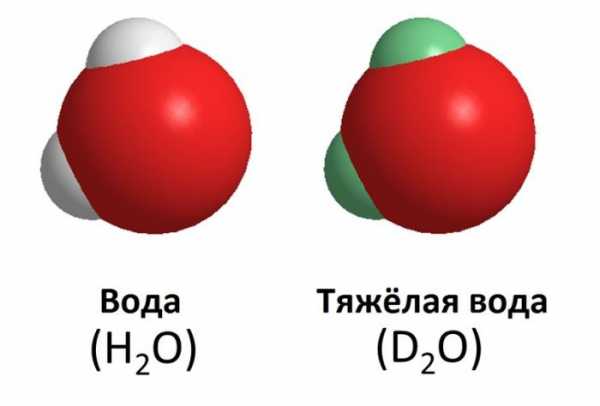 Формула простой и тяжелой воды
Формула простой и тяжелой водыДейтерий стабилен, довольно часто встречается в природе и содержится в воде, в том числе в тканях человека. Концентрация вещества мала, составляет 0,0156 %. Несмотря на это, его содержание в воде увеличивает плотность жидкости, тем самым делает воду тяжелой. В лабораториях такую воду получают путем электролиза и дистилляции, что ресурсозатратно и дорого. В больших масштабах получение D2O возможно методом Гербера, основанном на изотопном обмене.
Сходства и отличия обычной и обогащенной дейтерием воды
- По цвету тяжелая вода не отличается от обычной.
- По вкусу D2O сладковатая в отличие от обычной безвкусной.
- Ее плотность почти на 11 % выше плотности h3O, что делает ее более вязкой.
- D2O имеет большую температуру плавления и кипения.
Химические свойства дейтерия
Дейтерий — легкий газ, он легче воздуха. D2 отлично горит, температура короны исходящего пламени составляет 1 600 °С, поэтому огонь способен плавить стекло. Термические реакции с дейтерием не проводятся, так как в современных условиях важны более энергообъемные ядерные реакции, на которые элемент без сомнения способен.
 Из-за большой плотности D2O лед из нее тонет в обычной воде, что не наблюдается в случае с h3O
Из-за большой плотности D2O лед из нее тонет в обычной воде, что не наблюдается в случае с h3OПри реакции между атомами дейтерия образуется He3. Это фундаментальная реакция, так как по такому же принципу зажигаются протозвезды в процессе формирования, еще до выхода из стадии коррекционного диска. Ей же живут коричневые карлики. Именно на основе дейтерия в США создали первую атомную бомбу.
Можно ли пить тяжелую воду
Воду с химической формулой D2O можно пить при необходимости, так как она токсична в малой степени и через несколько дней весь дейтерий будет выведен из организма. В рамках опытов было выяснено, что первые 100-200 г могут вызвать вестибулярные нарушения.
Но если пить тяжелую воду несколько месяцев, то последствия могут быть плачевными. Замещение 25% водорода дейтерием у млекопитающих может привести к стерильности воды в тканях, что впоследствии приведет к минимальному энергообмену и смерти и часто это необратимо. При восстановлении функций жидкости последствиями может стать бесплодие. При концентрации h3O и D2O в пропорциях 1:1 организм млекопитающего, в том числе человека, погибает.
Рыбы и беспозвоночные могут существовать при содержании в организме 90% дейтерийсодержащей воды, простейшие с гетеротрофным типом питания — при 70%. Некоторые бактерии и водоросли способны существовать и размножаться в D2O.
Интересные факты о применении тяжелой воды
Во время Второй мировой войны большая часть трудов физиков-атомщиков уходила на создание ядерного оружия. В Германии его решили создавать из плутония.

Но чтобы получить этот изотоп, необходимо было облучать уран, а полученные нейтроны значительно замедлять. В качестве замедлителя подходил графит и тяжелая вода, но ни того, ни другого у немцев не было. Тогда они приняли решение построить в оккупированной Норвегии электролизную электростанцию. Груз с тяжелой водой они так и не получили, в 1943 г. паром затонул.
Реакторы на тяжелой воде нашли дальнейшее применение, так как в них можно использовать природный, а не обогащенный уран, хотя над получением воды тоже необходимо потрудиться. Сегодня несколько канадских реакторов продолжают работать на тяжелой воде.
что такое тяжелая вода и можно ли ее пить
Тем, чьи знания по химии ограничиваются объемом школьной программы, может казаться, что вода состоит только из монооксида водорода и имеет всем известную формулу h3O. Это так, но кроме него в состав могут входить изотопы Н: протий, дейтерий и тритий.
Тритий нестабилен, поэтому практически отсутствует в воде. При этом существующий сверхтяжелый водород распадается на гелий, излучая электрон и антинейтрино. Выделение значительного числа электронов может вызвать свечение люминофора вроде того, как светятся небольшие тритиевые брелки, в которых запечатан изотоп.
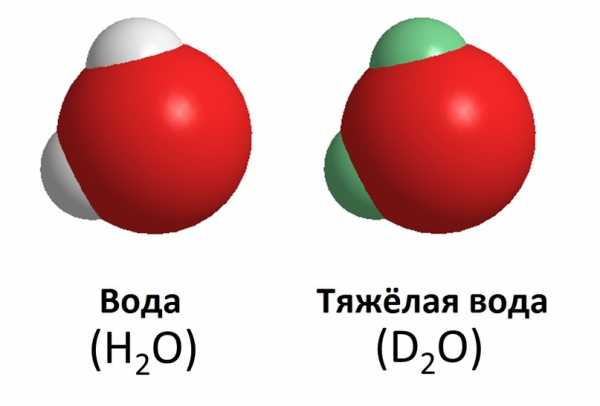 Формула простой и тяжелой воды
Формула простой и тяжелой водыДейтерий стабилен, довольно часто встречается в природе и содержится в воде, в том числе в тканях человека. Концентрация вещества мала, составляет 0,0156 %. Несмотря на это, его содержание в воде увеличивает плотность жидкости, тем самым делает воду тяжелой. В лабораториях такую воду получают путем электролиза и дистилляции, что ресурсозатратно и дорого. В больших масштабах получение D2O возможно методом Гербера, основанном на изотопном обмене.
Сходства и отличия обычной и обогащенной дейтерием воды
- По цвету тяжелая вода не отличается от обычной.
- По вкусу D2O сладковатая в отличие от обычной безвкусной.
- Ее плотность почти на 11 % выше плотности h3O, что делает ее более вязкой.
- D2O имеет большую температуру плавления и кипения.
Химические свойства дейтерия
Дейтерий — легкий газ, он легче воздуха. D2 отлично горит, температура короны исходящего пламени составляет 1 600 °С, поэтому огонь способен плавить стекло. Термические реакции с дейтерием не проводятся, так как в современных условиях важны более энергообъемные ядерные реакции, на которые элемент без сомнения способен.
 Из-за большой плотности D2O лед из нее тонет в обычной воде, что не наблюдается в случае с h3O
Из-за большой плотности D2O лед из нее тонет в обычной воде, что не наблюдается в случае с h3OПри реакции между атомами дейтерия образуется He3. Это фундаментальная реакция, так как по такому же принципу зажигаются протозвезды в процессе формирования, еще до выхода из стадии коррекционного диска. Ей же живут коричневые карлики. Именно на основе дейтерия в США создали первую атомную бомбу.
Можно ли пить тяжелую воду
Воду с химической формулой D2O можно пить при необходимости, так как она токсична в малой степени и через несколько дней весь дейтерий будет выведен из организма. В рамках опытов было выяснено, что первые 100-200 г могут вызвать вестибулярные нарушения.
Но если пить тяжелую воду несколько месяцев, то последствия могут быть плачевными. Замещение 25% водорода дейтерием у млекопитающих может привести к стерильности воды в тканях, что впоследствии приведет к минимальному энергообмену и смерти и часто это необратимо. При восстановлении функций жидкости последствиями может стать бесплодие. При концентрации h3O и D2O в пропорциях 1:1 организм млекопитающего, в том числе человека, погибает.
Рыбы и беспозвоночные могут существовать при содержании в организме 90% дейтерийсодержащей воды, простейшие с гетеротрофным типом питания — при 70%. Некоторые бактерии и водоросли способны существовать и размножаться в D2O.
Интересные факты о применении тяжелой воды
Во время Второй мировой войны большая часть трудов физиков-атомщиков уходила на создание ядерного оружия. В Германии его решили создавать из плутония.

Но чтобы получить этот изотоп, необходимо было облучать уран, а полученные нейтроны значительно замедлять. В качестве замедлителя подходил графит и тяжелая вода, но ни того, ни другого у немцев не было. Тогда они приняли решение построить в оккупированной Норвегии электролизную электростанцию. Груз с тяжелой водой они так и не получили, в 1943 г. паром затонул.
Реакторы на тяжелой воде нашли дальнейшее применение, так как в них можно использовать природный, а не обогащенный уран, хотя над получением воды тоже необходимо потрудиться. Сегодня несколько канадских реакторов продолжают работать на тяжелой воде.
Биологическое и медицинское действие тяжелой и легкой воды
Учитывая способность дейтерированной воды изменять скорость химических реакций и ее другие значительные отличия от протиевой воды, уже заранее можно было ожидать, что вода, богатая или бедная D или Т, будет оказывать сильное физиологическое действие.
Действительность превзошла все ожидания. Действие тяжелой и легкой волы оказалось многообразным и менее однозначным, чем можно было бы предположить a priori.
Рассмотрим сначала биологическое действие тяжелой воды D2О или (DHO). Первоначальные исследования обнаружили повреждающее действие тяжелой воды на биологические процессы вплоть до смерти живых организмов. Когда открыли D, то биологи задались вопросом, какое действие на организм оказывает дейтерий — вредное или полезное, а может быть, вообще не оказывает никакого действия?
Одним из первых этим вопросом занялся американский ученый Льюис. Он нашел, что в тяжелой воде высокой концентрации размножение микробов сильно задерживается: помутнение питательного бульона наблюдается лишь через две недели (контрольная пробирка мутнела за несколько часов).
Расщепление сахара дрожжами идет в тяжелой воде в 9 раз медленнее. Некоторые простейшие и коловратки погибают в тяжелой воде.
Действие энзимов сильна задерживается. Ричардс обнаружил, что дрожжи в тяжелой воде растут гораздо медленнее. Паксу установил, что скорость выделения углекислого газа при брожении альфа-глюкозы под влиянием дрожжей в чистой D2O в 9 раз меньше, чем в чистой Н2О, а в 60%-ной D2O — в 1,6 раза меньше.
Семена табака не прорастают в тяжелой воде, в 50-ной D2O они прорастают вдвое медленнее по сравнению с обычной водой. Если семена из тяжелой воды перенести в обычную, то часть из них через неделю начинают прорастать, хотя и не вполне нормально.
Плоские черви вида планария макулета за 1-2 часа пребывания в теряли всякие признаки жизни. После того как их переносили в обычную воду, только часть из них через несколько часов начинали приходить в норму, остальные погибали. Для головастиков и мальков 40-часовое пребывание в 92 и даже в 30%-ной D2O оказывалось смертельным. Интересно отметить то обстоятельство, что, в то время как в большой концентрации тяжелая вода смертельна для рыб, головастиков и червей, инфузория парамеция жила в этих условиях 24 часа. Во время этих исследований было также замечено, что белые мыши, которых поили тяжелой водой, обнаруживали крайнее беспокойство, выражающее острую жажду.
Когда развивается какое-нибудь новое научное направление, то обычно в первую очередь замечаются и исследуются прямолинейные зависимости, как, например, в данном случае: тяжелая вода — яд. Но со временем накапливаются факты, не укладывающиеся в первоначальные примитивные схемы, выясняется, что есть какие-то противоречия. Именно на них — противоречиях — должно быть сосредоточено главное внимание. Они либо открывают глаза на допущенные ранее ошибки, на невольное преувеличение значения отдельных факторов, либо проясняют более глубокую и тонкую структуру явлений и переводят этим самым исследование на более высокую ступень достоверности и убедительности. Так было и при изучении влияния дейтерия на жизнедеятельность организмов, сопровождавшемся борьбой противоположных мнений.
Так, например, с утверждением, что дейтерий — яд, был не согласен крупный биохимик Бэрнс. Поместив водоросль — спирогиру в воду с повышенным содержанием дейтерия, он наблюдал то же замедленное движение клеток и прекращение их деления, но сделал из этого совершенно противоположный вывод. По его мнению, такое поведение клеток говорит не о старении организмов, а об увеличении продолжительности жизни.
И.П.Григоров прямо утверждает, что тяжелая вода не ядовита. Для доказательства такой точки зрения он провел в общем-то очень интересный опыт. Жир, в котором часть протия была замещена дейтерием, скармливался мышам. Оказалось, что дейтерированный жир быстро попадает в запас, в жировое депо. Одновременно из депо уходит обычный, протиевый жир. За три дня таким образом обновляется 2/3 жирового запаса депо. Такой процесс вполне соответствует пониженной химической активности дейтериевых соединений. Обратный обмен меченного дейтерием жира из запаса на обычный жир, поступающий с пищей, проходил с такой же скоростью. Но подопытные мыши остались живы, здоровы и активны. Жаль, что эти опыты не были продолжены на срок более трех суток. Длительные опыты, наверное, рассеяли бы заблуждения о безвредности дейтерия.
Да что говорить о безвредности, если Уэпер в своих экспериментах нашел, что тяжелая вода в небольших количествах определенно стимулирует рост и развитие плесневого грибка аспергиллус! Н.А.Шишаков добавляет, что так же действует тяжелая вода и на спирогиру, и на дрожжевой грибок сахаро-мицес перевизае. Махт и Дэвис считают, что вода, содержащая 0,2% D2O, не отличается по физиологическому действию от обыкновенной воды. Хотя некоторые простейшие и коловратки погибают в D2O, но евглена и целый ряд бактерий при возвращении в обычную воду оживают вновь. На клетки элодеи D2O окаэывавет очень медленное действие.
Страницы: 1 2 3 4 5 6 7 8
Ответы Mail.ru: Как делают тяжелую воду?
кидайте в неё всё что есть под рукой
<a rel="nofollow" href="http://works.tarefer.ru/89/100199/index.html" target="_blank">http://works.tarefer.ru/89/100199/index.html</a>
В домашних - нельзя ... Способ-то достаточно простой - тяжелая вода кипит при температур чуть выше, чем простая, но в домашних условиях воспроизвести процесс просто нереально
Да, возможно. Нужно в 1 литр воды бросить 1 кг свинца.:)))
Тяжёлая вода́ (также оксид дейтерия) — обычно этот термин применяется для обозначения тяжёловодородной воды. Тяжёловодородная вода имеет ту же химическую формулу, что и обычная вода, но вместо атомов обычного лёгкого изотопа водорода (протия) содержит два атома тяжёлого изотопа водорода — дейтерия. Формула тяжёловодородной воды обычно записывается как D2O или ²h3O. Внешне тяжёлая вода выглядит как обычная — бесцветная жидкость без вкуса и запаха. яжёлая вода токсична лишь в слабой степени, химические реакции в её среде проходят несколько медленнее, по сравнению с обычной водой, водородные связи с участием дейтерия несколько сильнее обычных. Эксперименты над млекопитающими показали, что замещение 25 % водорода в тканях дейтерием приводит к стерильности, более высокие концентрации приводят к быстрой гибели животного. Однако некоторые микроорганизмы способны жить в 70 % растворе D2O в h3O (простейшие) и даже в чистой тяжёлой воде (бактерии) . Человек может без всякого вреда для здоровья выпить несколько стаканов тяжёлой воды, весь дейтерий будет выведен из организма через несколько дней. Таким образом, тяжёлая вода гораздо менее токсична, чем, например, поваренная соль. Тяжёлая вода накапливается в остатке электролита при многократном электролизе воды. На открытом воздухе тяжёлая вода быстро поглощает пары обычной воды, поэтому можно сказать, что она гигроскопична. Производство тяжёлой воды очень энергоёмко, поэтому её стоимость довольно высока (ориентировочно 200—250 долларов за кг) . Среди населения бытует миф о том, что при длительном кипячении природной воды концентрация тяжёлой воды в ней повышается, что якобы может вредно сказаться на здоровье. В действительности же повышение концентрации тяжёлой воды при кипячении ничтожно (к тому же тяжёлая вода практически не ядовита) . Производство тяжёлой воды очень энергоёмко, поэтому её стоимость довольно высока (ориентировочно 200-250 долларов за кг) . В настоящее время разработан ряд эффективных методов получения тяжелой воды: электролизом, изотопным обменом, сжиганием обогащенного дейтерием водорода.
Синтезируют изотоп водорода - дейтерий
Полезна ли тяжёлая вода?
Сообщение:
Добрый день Только что прочел у вас статью или ответ на вопрос читателя о том , что оказываетья тяжелая вода в меньших количествах полезна... Но если это действительно так, то почему при приготовлении талой воды, при замораживании вы рекомендуете убрать ледяную корочку которая формируется вначале. Это вы говорите именно тяжелая замораживается первой и ее необходимо убрать. Но раз она полезна как ты потом пишете, зачем ее убрать? Может оставить раз так полезна?
Спасибо
______________
Здравствуйте!
В статье про тяжёлую воду, на которую вы ссылаетесь, действительно была ссылка на то, что по мнению некоторых исследователей небольшие количества тяжёлой воды оказывают положительный эффект на скорость протекания некоторых ферментативных реакций. При этом концентрации тяжёлой воды в среде составляют 0,1%. Природа этого феномена окончательно не изучена. Возможно, это связано с изотопными эффектами, которые для дейтерия могут быть значительными. Двукратным увеличением массы дейтерона относительно протона и обуславливаются так называемые изотопные эффекты тяжёлой воды - энергия связи, константа диссоциации, подвижность, длина связи и т.д. Связи, сформированные атомами дейтерия прочнее водородных связей. Различия в нуклеарной массе атома водорода и дейтерия косвенно могут служить причиной различий в синтезах нуклеиновых кислот, которые могут приводить в свою очередь к структурным различиям и, следовательно, к функциональным изменениям в клетке. Всё это приводит к тому, что именно ферментативные системы, которые используют высокую подвижность протонов и высокую скорость разрыва протонных связей, наиболее чувствительные к замене Н+ на D+.
При этом клетки животных способны выдерживать до 25-30% тяжёлой воды в среде, растений (50%), а клетки простейших микроорганизмов способны жить на 80% тяжелой воде. Нами показано, что способность к адаптации в высоких концентрациях тяжёлой воды связана с эволюционным уровнем организации, т. е. чем ниже уровень развития живого, тем выше способность к адаптации (О.В. Мосин, Д.А. Складнев, В.И. Швец, 1996). Изменения соотношения основных метаболитов в процессе адаптации к тяжеловодородной среде также может являться причинами гибели клеток. Клетки высших организмов погибают при содержании тяжёлой воды в составе тела свыше 30%, но микроорганизмы, легко приспосабливающиеся к резким изменениям среды обитания, способны жить и размножаться даже в 98%-ной тяжёлой воды (Мосин О.В, 1996).
В общем плане тяжёлая вода высокой концентрации токсична для организма; химические реакции в её среде проходят несколько медленнее, по сравнению с обычной водой, водородные связи с участием дейтерия несколько сильнее обычных.
Тем не менее тяжелая вода играет значительную роль в различных биологических процессах. Различные исследователи, что тяжелая вода действует отрицательно на жизненные функции организмов; это происходит даже при использовании обычной природной воды с повышенным содержанием тяжелой воды.
Влияние концентрации дейтерия на рост высших растений

Подопытных животных поили водой, 1/3 часть которой была заменена водой состава HDO. Через недолгое время начиналось расстройство обмена веществ животных, разрушались почки. При увеличении доли тяжелой воды животные погибали.
На развитие высших растений тяжелая вода также действует угнетающе; если их поливать водой, на половину состоящей из тяжелой воды, рост прекращается.

Рис. Поливка помидорной рассады 30, 50 и 60%-ной тяжёлой водой ингибирует рост растения (по данным Креспи и Катца, 1972).
В общих чертах, при попадании клеток в дейтерированную тяжёловодородную среду из них не только исчезает протонированная вода за счет реакции обмена Н2О-D2О, но и происходит быстрый H±D обмен в гидроксильных, сульфгидрильных и аминогруппах всех органических соединений, включая белки, нуклеиновые кислоты, липиды, сахара. Только С—Н-связь не подвергается обмену и соединения типа С—D синтезируются «de поvo».
Интересно, что после обмена H±D ферменты не прекращают своей функции (Themson et al., 1966; Денько, 1974), но изменения в результате изотопного замещения за счет первичного и вторичного изотопных эффектов (Thomson, 1963; Halevy, 1963), а также действие тяжёлой воды как растворителя (большая структурированность и вязкость по сравнению с обычной водой) приводят к изменению скоростей и специфичности ферментативных реакций в тяжёлой воде.
Также не исключается, что эффекты, наблюдаемые при помещении клеток в тяжёлую воду связаны с образованием в тяжёлой воде конформаций молекул с иными структурно-динамическими свойствами, чем конформаций, образованных с участием водорода, и поэтому имеющих другую активность и биологические свойства. Так, по теории абсолютных скоростей разрыв СH-связей может происходить быстрее, чем СD-связей, подвижность иона D+ меньше, чем подвижность Н+, константа ионизации тяжёлой воды меньше константы ионизации обычной воды. Всё это отражается на кинетике химической связи и скорости химических реакций в тяжёлой воде.
Связи, образованные атомами углерода с дейтерием немного прочнее, чем СН-связи из-за того, что частота колебания дейтерона, имеющего большую массу (в два раза большую, чем протон) и размер меньше частоты колебания протона и тем самым, это стабилизирует связь.
Другое важное свойство определяется самой пространственной структурой тяжёлой воды, которая имеет тенденцию сближать гидрофобные группы макромолекулы, чтобы минимизировать их эффект на водородную (дейтериевую) связь в присутствии молекул тяжёлой воды. Так что структура спирали, каковой является ДНК в присутствии тяжёлой воды стабилизируется.
Кроме этого, отмечены радиопротекторные свойства тяжёлой воды на клетки печени обезьяны, в которой экспонировались эти клетки. Также было показано, что жизненный цикл плоских червей, выращенных на тяжёлой воде увеличивается в 1.5 раза по-сравнению с червями, выращенными на обычной воде (М. Шепенинов, 2006). Это объясняется тем, что связи, образованные дейтерием прочнее таковых, образованных с участием водорода, поэтому они меньше рвутся и менее подвержены мутациям и другим внешним воздействиям.
Имеются и другие положительные эффекты тяжёлой воды, которые могут быть очень ценными, например, для получения термостабильных дейтерированных ферментов, способных работать при высоких температурах. Но это пока только предположения. Сам я никогда не утверждал, что тяжёлая вода полезна для организма. Имелось в виду положительное влияние сверхмалых концентраций дейтерия на некоторые наиболее чувствительными к замене Н+ на D+ ферментативные системы и биосинтетические процессы, протекающие в клетке - транспорт веществ и др., т. е. те, которые используют высокую подвижность протонов и высокую скорость разрыва протонных-дейтериевых связей.
К.х.н. О. В. Мосин
почему тяжело пить 2л воды? кто это делает легко в течение дня?
Ты себя насильно не заставляй. Как правило, нельзя сидеть за компом, и хлестать воду, так она в любом случае вылезет (проверено мною) Ты иди на улицу, и побееегай минуточек двадцать, что аж дыхание перехватило, приди домой, и налей стаканчик прохладной воды (не холодной!!! ) поскольку после физ. нагрузок пить захочешь от выделения пота. Выпьешь стакан воды - облегчение, да?? ? Это первый секрет. Второй - во время еды воду не пей - вредно. Поешь, подожди минут 30, и только тогда пей воду, чай, компоот, и т. д. Третий секрет - воду вечером не пей, лучше больше пей воды с пробуждением, в первой половине дня, поскольку так вода усвоится лучше и полезней будет. Удачи)) Я вот уже с удовольствием каждые полчаса полстакана выпиваю))
не надо целый стакан за раз выпивать.. в течение дня маленькими глоточками надо пить воду.
У меня на столе (работаю из дома) стоит двух литровая бутылка из-под аква минерале, утром выливаю туда воду из чайника, в течение дня как захочется пить - делаю пару глотков. Бывает же, что лень идти кофе заваривать, или сильно заработаешься - не отвлечься. За день вся бутылка и уходит как-то незаметно.. . :)
пей гранатовый сок - его легко пить
ну так не одну же воду пить надо что-то есть а чтобы хотелось пить советую купить рыбу соленую сушеную или кальмары. можно купить икру из водорослей или сами водорости в банках да любые соленые морепродукты от них пить хочется, только не консервированные.
Трудно сказать почему трудно, тому, кто с лёгкостью это делает. Мы же никогда с этой трудностью не сталкивались.
Если кипяченную воду кипятить снова и снова... называется ли такая вода "тяжелая вода" и вредно ли это?
нет! кипячением нельзя получить яжёлую воду! и это не вредно! а вот вам поподробнее: До XIX века люди считали воду обычным химическим элементом. В 1805 году Александр Гумбольдт и Жозеф Луи Гей-Люссак установили, что вода состоит из молекул, каждая из которых содержит два атома водорода и один кислорода и считалось, что вода - индивидуальное соединение, описываемое единственно возможной формулой. В 1932 году мир облетела сенсация: кроме воды обычной, в природе существует еще и тяжелая вода. В небольших количествах тяжелая вода постоянно и повсеместно присутствует в природных водах, которую от обычной воды можно различить лишь по физическим характеристикам. В молекулу тяжелой воды входят атомы не легкого водорода - протия (1H), а его тяжёлого изотопа - дейтерия (2D), атом которого на единицу тяжелее протиевого, а молекулярный вес тяжелой воды на 2 единицы больше: 20, а не 18. Тяжёлая на 10% плотнее обычной Тяжелая вода в природе находится в небольших количествах - в миллионных долях процента. Преобладает ее разновидность, состав которой выражается формулой HDO. В Мировом океане содержится 1015 тонн HDO. Тяжелая вода - очень важное промышленное сырье для атомной энергетики, эффективный замедлитель быстрых нейтронов. Подопытных животных поили водой, 1/3 часть которой была заменена водой состава HDO. Через недолгое время начиналось расстройство обмена веществ животных, разрушались почки. При увеличении доли тяжелой воды животные погибали. На развитие высших растений тяжелая вода также действует угнетающе; при поливе их водой, на половину состоящей из тяжелой воды, рост прекращается. Но всё же несмотря на это многие клетки бактерий, растений и водорослей могут быть адаптированы к росту на тяжёлой воде. Пониженное содержание дейтерия в воде стимулирует жизненные процессы. При потреблении воды с содержанием дейтерия на 25% ниже нормы свиньи, крысы и мыши дали потомство, гораздо многочисленнее и крупнее обычного, яйценоскость кур поднялась вдвое, пшеница созрела раньше и дала более высокий урожай. Это может быть объяснено разницей в плотности и вязкости тяжёлой воды, а также её гидрофобными эффектами. Позднее, при выяснении фракционного состава воды была обнаружена сверхтяжелая вода Т20. В ее составе место водорода занимает его природный изотоп, еще более тяжелый, чем дейтерий. Это тритий (Т) , который в отличие от дейтерия он радиоактивен, атомная масса его равна 3. Тритий зарождается в высоких слоях атмосферы, где идут природные ядерные реакции. Он является одним из продуктов бомбардировки атомов азота нейтронами космического излучения. Ежеминутно на каждый квадратный сантиметр земной поверхности падают 8- 9 атомов трития. В небольших количествах сверхтяжелая (тритиевая) вода попадает на Землю в составе осадков.
нет это не тяжёлая вода. вредно
дейтерий и тритий-это молекулы водорода с массой 2 и 3 вместо 1 у норм. изотопа. кипячением такую воду не получить..
Вероятно, ты имеешь в виду, что при длительном кипячении должен получиться дейтерий? Если бы его можно было получить ТАК просто, то не нужно было бы строить дорогущие мощные химические реакторы.. . Не обольщайся - дейтерий в чайнике ты не получишь...
не тяжёлая, скорее убитая
тяжёлая вода - это тритий (водород, поддавшийся бета-излучению) , вроде
Ответ Zilola достаточно полный и точный. А кипятить воду многократно не вредно, но бесполезно.
Собственно тяжелую и полутяжелую воду ты так не выделишь, но их концентрацию, несомненно, повысишь. Что касается вредности, да нет, не особо. Какая разница, выпьешь ты стакан с одной концентрацией или одну десятую - с большей, вода - она вода и есть, пусть и с чуть иными физическими свойствами.
Без разницы. Супы неделю едим, кипятим.
Тяжёлая вода токсична лишь в слабой степени, химические реакции в её среде проходят несколько медленнее, по сравнению с обычной водой, водородные связи с участием дейтерия несколько сильнее обычных. Эксперименты над млекопитающими показали, что замещение 25 % водорода в тканях дейтерием приводит к стерильности, более высокие концентрации приводят к быстрой гибели животного. Однако некоторые микроорганизмы способны жить в 70 % растворе D2O в h3O (простейшие) и даже в чистой тяжёлой воде (бактерии) . Человек может без видимого вреда для здоровья выпить стакан тяжёлой воды, весь дейтерий будет выведен из организма через несколько дней. Таким образом, тяжёлая вода гораздо менее токсична, чем, например, поваренная соль. Тяжёлая вода накапливается в остатке электролита при многократном электролизе воды. На открытом воздухе тяжёлая вода быстро поглощает пары обычной воды, поэтому можно сказать, что она гигроскопична. Производство тяжёлой воды очень энергоёмко, поэтому её стоимость довольно высока (ориентировочно 200—250 долларов за кг) . Среди населения бытует миф о том, что при длительном кипячении природной воды концентрация тяжёлой воды в ней повышается, что якобы может вредно сказаться на здоровье. В действительности же повышение концентрации тяжёлой воды при кипячении ничтожно (к тому же тяжёлая вода практически не ядовита) .
читай здесь: <a rel="nofollow" href="http://n-t.ru/tp/mr/otv.htm" target="_blank">http://n-t.ru/tp/mr/otv.htm</a> если лень всё читать, то суть в следущем: Если мы откроем водопроводный кран и наберем чайник, то там будет не однородная вода, а ее смесь. При этом дейтериевых «вкраплений» окажется очень немного – примерно 150 граммов на тонну. Получается, что тяжелая вода есть повсюду – в каждой капле! Проблема в том, как ее взять. Ныне во всем мире ее добыча связана с огромными затратами энергии и очень сложным оборудованием. <...> А вместе с тем известно, что физико-химические свойства D2O совсем иные, чем у Н20 – ее постоянного спутника. Так, температура кипения тяжелой воды +101,4°С, а замерзает она при +3,81°С. так что если чайник не перегревать выше 101.4, то вся лёгкая вода выкипит, и останется тяжёлая (теоретически).
польза и вред, как пить, можно ли из источника, а также есть ли противопоказания
Разрешено ли употреблять сульфидную воду?
 Сероводородная вода используется (в т.ч. вовнутрь). при лечении многих болезней, обычно в санаториях.
Сероводородная вода используется (в т.ч. вовнутрь). при лечении многих болезней, обычно в санаториях.
В ней есть:
- хлористый натрий,
- магний,
- кальций.
Сероводород содержится в виде сернокислых солей – сульфитов. Они придают воде кислотность и лечебные свойства.
Если таких солей много, она становится мыльной и сильно пахнет тухлыми яйцами. Такая вода используется только наружно.
Сероводород проникает через кожу, расширяя сосуды и раздражая нервные окончания. Такую воду можно применять для компрессов, орошения, ингаляций. Употреблять сульфидные минеральные воды можно для питьевого лечения, если сульфитов в ней немного.
В каких случаях все-таки допускается?
Сульфидная вода содержит разное количество солей сероводорода. Для приема внутрь разрешено принимать такие, где их не более 40 мг/л. Они оказывают сильное воздействие на организм, поэтому допускается их пить только по назначению врача.
Популярны такие разновидности:
- Баталинская;
- Кашин;
- Московская;
- Ивановская;
- Шаамбары.
 Известные источники есть в:
Известные источники есть в:
- Мацесте,
- Пицунде,
- Пятигорске,
- Кындыге и на других курортах.
Но концентрация сероводорода в тех водах очень высока, может составлять до 300 мг/л. Поэтому их используются только наружно.
Употреблять внутрь можно только сульфидные воды из минеральных источников.
Если из скважины в доме ощущается запах тухлых яиц, пользоваться ей нельзя. Такой сероводород токсичен и может привести к отравлению.
Польза и вред
Назначать прием сульфидной воды может только специалист. Ее употребляют при различных заболеваниях желудочно-кишечного тракта, интоксикации.
Она обладает такими свойствами:
- уменьшает секрецию желудочного сока;
- стимулирует выработку желчи и ее выведение;
- выводит токсины, соли тяжелых металлов;
- повышает иммунную защиту;
- помогает уменьшить воспалительные процессы;
- ускоряет метаболизм;
- снижает количество глюкозы и холестерина в крови;
- успокаивает, устраняет раздражительность.
Назначается такое лечение даже детям и подросткам для укрепления иммунитета и улучшения работы сердечно-сосудистой системы. Но сероводородная вода может принести вред при неправильном применении. Она создает большую нагрузку на сердце, нервную систему.
Высокие концентрации сероводорода вызывают аллергические реакции. Особенно часто негативные последствия проявляются у истощенных, ослабленных больных, после тяжелых нагрузок, у тех, кто курит или злоупотребляет алкоголем.
Наличие сероводорода в водопроводной воде приводит к тяжелому отравлению. Его первые признаки – тошнота, головокружение, головные боли.
Противопоказания
Так как сероводород – это токсичный газ, такие воды можно пить не всем. Запрещено лечение такой водой в следующих случаях:
- при туберкулезе;
 при почечной недостаточности;
при почечной недостаточности;- наличии опухолей;
- нарушении сердечного ритма;
- при варикозном расширении вен;
- склонности к кровотечениям;
- гипотонии;
- при обострении заболеваний желудочно-кишечного тракта;
- нарушении мозгового кровообращения;
- склонности к аллергическим реакциям;
- бронхиальной астме.
Нельзя употреблять сульфидные воды женщинам при беременности и во время кормления грудью. А детям их дают только с 7 лет и под наблюдением врача.
Как правильно употреблять?
Сероводородные воды даже с небольшим содержанием сульфидов оказывают сильное воздействие на организм. Поэтому употреблять их можно только в дозах, рекомендуемых врачом. Нельзя менять, особенно увеличивать дозировку.
Наиболее эффективным является такое лечение на курорте. Там на больного воздействуют разные целебные факторы, а вода употребляется нужной температуры.
 Необходимо пить ее, нагрев предварительно до температуры 37°. Во время нагревания удаляются газы, которые могут привести к метеоризму и спазмам в кишечнике.
Необходимо пить ее, нагрев предварительно до температуры 37°. Во время нагревания удаляются газы, которые могут привести к метеоризму и спазмам в кишечнике.
Принимать такую минералку нужно, начиная с четверти стакана, постепенно доводя до целого.
Можно выпивать 1-2 стакана каждый день, лучше делать это за полчаса до приема пищи. Пить нужно медленно, небольшими глотками. Длительность терапии составляет 2-4 недели.
Заключение
Сульфидные воды – это эффективное средство для лечения многих болезней. Но пить можно только воду из минеральных источников с небольшой концентрацией сероводорода. Перед этим обязательно проконсультироваться со специалистом.
Можно ли пить жесткую воду - на что решиться?
Каждый сталкивался с ситуацией, когда от накипи в чайнике, отложений на бытовой технике, трубах, котлах, оборудование приходило в негодность, причина тому – жесткая вода. Если она убивает бытовую технику наповал, то можно ли пить жесткую воду, как она влияет на самочувствии и здоровье человека?
Бесспорно, жесткость проявляется не везде. В каждом конкретном случае, регионе, стране существуют источники жесткой воды. Данное определение является характерной чертой для воды, даже после процесса водоподготовки к питью в системах централизованного водоснабжения.
Решения BWT для умягчения воды:
Жесткость формируется в результате растворения минералов и химических элементов еще на первоначальных стадиях формирования воды, в горных породах. Большая часть - это магний и кальций, данные химические элементы встречаются в известняке, доломите, меле. Говоря научным языком, жесткая вода – это совокупность физических свойств воды, напрямую зависящих от содержания в ней солей щелочноземельных металлов. В быту необходимо проверять и контролировать жесткость воды независимо от источника (родник, скважина) и осуществлять умягчение воды. Жесткость воды напрямую влияет на вкусовые свойства, при употреблении чувствуется горьковатый вкус, при умывании образуется эффект стянутости кожи, при использовании мыла плохо образуется пена.
Впервые о жесткости воды заговорили в Германии в XIX веке. Именно в тот период Герцогство Саксон-Веймарское приняло нормативы по контролю жесткости воды. В настоящее время показатель жесткости не должен превышать 7 мг/л. Различают два вида жесткости: временную и постоянную. Если временную можно одолеть посредством кипячения воды, в процессе которого образуется осадок (накипь), то с постоянной бороться практически невозможно. Если мы выяснили причины возникновения жесткости, то остается открытым единственный вопрос, можно ли пить жесткую воду?
Организм человека требует живую воду, с ее природной структурой, физиологически полноценной по своему составу. Основные макроэлементы жесткости воды необходимы человеку, поэтому пить жесткую воду можно. Рассмотрим влияние химических элементов на здоровье человека.
Магний способствует активизации ферментов углеводного обмена, элемент является участником образования белков, играет важную роль при высвобождении энергии аденозитрифосфата, снижает возбудимость нервных клеток, расслабляет сердечную мышцу. Суточная норма – 500-700 мг. Отсутствие необходимого количества магния в организме приводит к развитию сердечнососудистых заболеваний, гипертонии, некоторых кожных заболеваний, судорог, уролитиаза.
Кальций формирует и поддерживает костную ткань, структуру человека, контролирует ритм сердца, работает фильтром при свертывании крови, образовании мочи, повышает иммунитет, поддерживает баланс кислотно-щелочной среды, расслабляет мышцы, обладает антигистаминным свойством. Нехватка кальция в организме влияет на мужское бесплодие, нарушается естественное развитие и оплодотворение яйцеклетки. Кальций омолаживает, придает коже блеск, здоровый вид, укрепляет нервную систему. Суточная норма – 600-1000 мг. Рассмотрев факторы влияния минералов и химических элементов на человека, можно с уверенность ответить на вопрос, можно ли пить жесткую воду – можно пить.
Но, всему есть мера. Количество потребляемых минеральных веществ из воды должно быть в норме, без излишков. Частое употребление жесткой воды может привести к нарушению пищеварительной системы человека, образованию мочекаменной болезни, поэтому следует применять фильтры умягчители. В противовес жесткой воде можно привести в пример дистиллированную воду, при частом употреблении которой могут появиться предпосылки сердечнососудистых заболеваний. Специалисты утверждают, что постоянное употребление дистиллированной воды может привести к солевому дисбалансу организма, такая жидкость, если человек много ее пьет, вымывает все полезные вещества из организма.
При желании употребления питьевой воды со сбалансированной жесткостью следует покупать бутилированную воду. Информация о составе, жесткости воды должна присутствует на этикетке. 3,5 мг/л является отличным уровнем для показаний мягкости воды.
Смотрите также: